随着 FDA 设立多个特殊通道,以加速解决尚未满足的医疗需求以来,几十年间,创新在监管层面得以加速,“抢时间、争速度”成为了无数新药逐梦者的共识。
据统计,过去十几年间获 FDA 特殊认定的创新疗法数量正稳步上升。
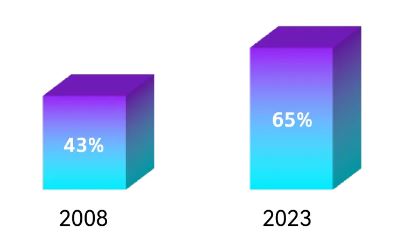
相较于常规审评模式,基于特殊通道审评的创新疗法,从IND到NDA的推进速度也正逐渐变快。
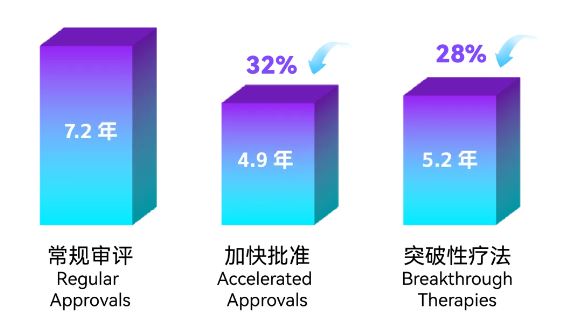
数据来源:参考资料[1]
当创新分子在发展
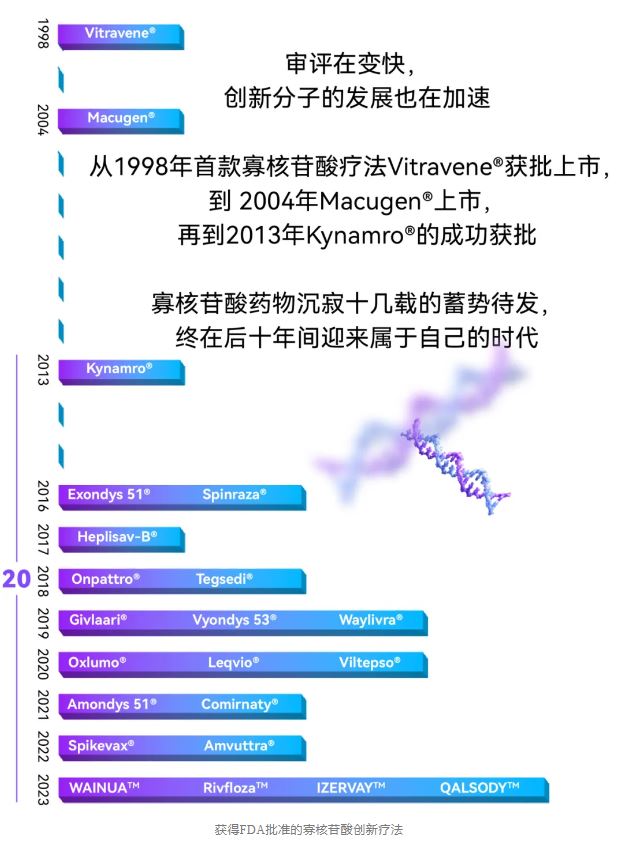
寡核苷酸药物肝靶向“明星” miRNA-GalNAc
2023 年 4 款获批的寡核苷酸疗法中,2 款使用 GalNAc 作为关键配体,以促进其与肝细胞中的唾液酸糖蛋白受体(ASGPR)相互作用[2]。
截至目前,FDA 共批准的 6 款 siRNA 上市药物中,5 款递送系统均为 GalNAc[3]。这些,让我们看到了 GalNAc 共轭偶联技术对解决寡核苷酸药物靶向性差、脱靶效应严重、稳定性差的重要贡献。
siRNA-GalNAc,WuXi TIDES 的快速交付策略
GalNAc 单体寡核苷酸偶联化合物的快速推进,对于研发生产平台的集成能力要求极高。在某真实案例中,WuXi TIDES 多个团队在 10 个月内,将一个用于治疗罕见病的 siRNA-GalNAc 候选化合物顺利推进至 IND 阶段。
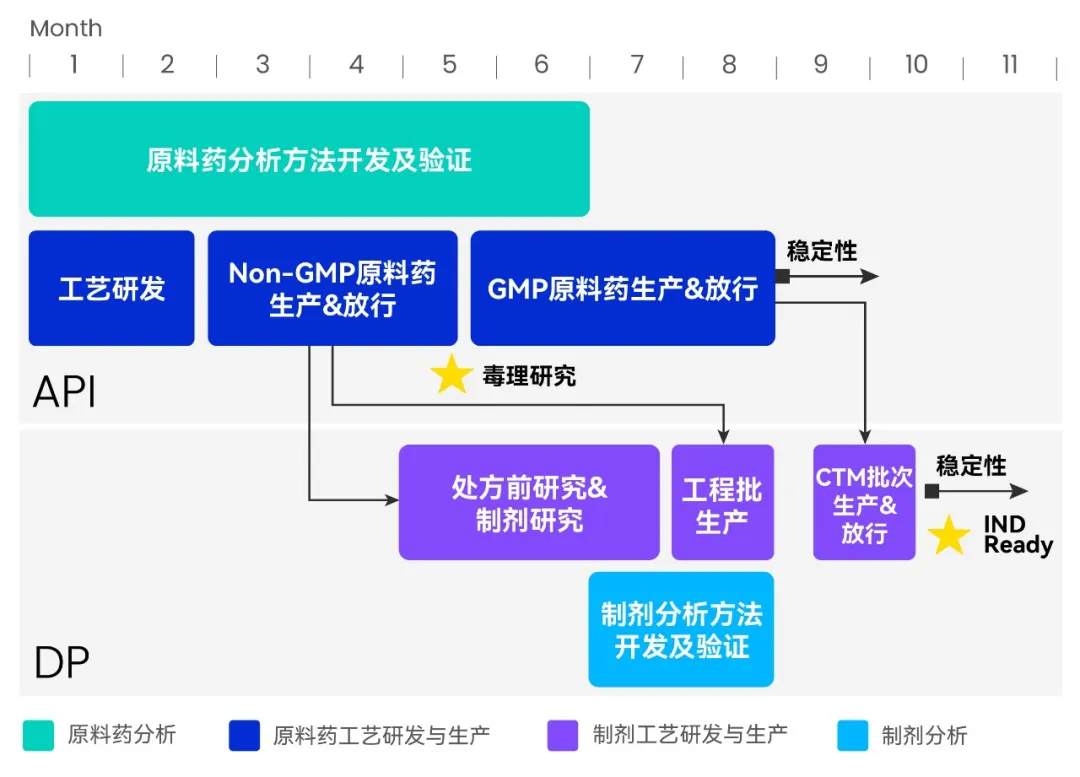
研发多线并行,生产无缝衔接
一、内部团队高质量合成 GalNAc 单体,确保偶联过程中原料质量与供应的稳健性
- 95%:GalNAc 单体纯度
- 3 倍:总收率提高,单批次可生产> 1 kg GalNAc 单体
- 流动化学:制备叠氮侧链,解决工艺放大潜在安全问题
二、快速、高质量且稳健的原料药工艺路线开发
- 6周:工艺路线开发
- 77%:粗品纯度
- 43%:收率
- 10周:完成 600 克 GMP API 生产
三、平行推进制剂研究,控制制剂生产时的原料药生产损耗
- <1 %:原料药损耗 (Line loss)
- 3 个月:早期阶段制剂研发
- 6 周:注射剂临床批生产、包装、贴标与放行
四、一体化模式下统一的质量体系,原料药分析方法直接转移至制剂
该项目原料药分析方法经验证后直接用于制剂研发,不仅简化CMC过程中的方法验证、减少相应资源与时间的投入、更为质量连续性提供保障。
平台能力全解锁,全面赋能有支撑
除了各团队高效执行的“软实力”,公司平台这类“硬实力”同样不可或缺:
一、定制化 GalNAc 服务赋能寡核苷酸药物开发
- 100+ GalNAc 化合物合成,覆盖不同类型的 GalNAc 分子
- 优化 GalNAc 树脂负载工艺,将固相合成的收率提高 50%
二、全面的寡核苷酸偶联能力
偶联类型
- 多肽-寡核苷酸,GalNAc-寡核苷酸,胆固醇-寡核苷酸,活性连接子-寡核苷酸等
偶联化学
- 酰胺键形成或点击化学
- 完成超滤和渗滤(UF&DF)后,在温和的水相条件下直接偶联
化学修饰策略
- 5’ 端:酰胺化修饰
- 3’ 端:定制固相载体修饰
- 寡核苷酸原料药
- 注射剂
- 分析
参考资料:
[1] Use of Expedited Regulatory Programs and Clinical Development Times for FDA-Approved Novel Therapeutics, JAMA Network Open. 2023
[2] Al Shaer D, Al Musaimi O, Albericio F, de la Torre BG. 2023 FDA TIDES (Peptides and Oligonucleotides) Harvest. Pharmaceuticals (Basel). 2024 Feb 13;17(2):243. doi: 10.3390/ph17020243. PMID: 38399458; PMCID: PMC10893093.
[3]《生物分析 | siRNA获批药物临床前毒性总结》Retrieved on Aug 1, 2024, from https://zhuanlan.zhihu.com/p/680891518




